
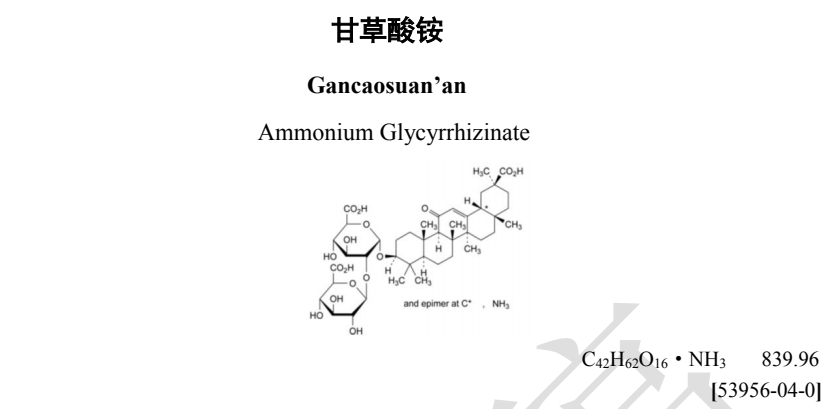
本品为 18α-甘草酸铵和 18β-甘草酸铵的混合物,主要成分为(20β)-3β-[2-O-(β-D -吡喃葡萄糖醛酸基)-α-D -吡喃葡萄糖醛酸基] 氧基-11-氧代齐墩果-12-烯-29-酸的铵盐。以无水与无乙醇物计算,含 C42H62O16·NH3 应为 78.0%~102.0%,其中含 18α-甘草酸铵不得过13.0%。
【性状】 本品为白色至浅黄色粉末或颗粒。比旋度 取本品约 0.5g,精密称定,置 50ml 量瓶中,加 50%乙醇溶解并稀释至刻度,摇匀。在 25℃时,依法测定(通则 0621),按无水无乙醇物计算,比旋度应为+49.0°至+55.0°。
【鉴别】
(1)取本品约 0.2g 于 10ml 试管中,加入 1mol/L 氢氧化钠溶液 1ml,振摇,产生的气
体能使湿润的红色石蕊试纸变蓝色。
(2)在含量测定项下记录的色谱图中,供试品溶液中 18α-甘草酸和 18β-甘草酸峰的保
留时间分别与系统适用性溶液中相应峰的保留时间一致。
(3)取本品适量,平铺于称量瓶中(厚度约 1mm),置温度为 25℃,相对湿度约为90%的条件下放置 24 小时后,置温度为 25℃,相对湿度约为 20%的条件下再放置 24 小时,
依法测定(通则 0402)。本品的红外光吸收图谱应与甘草酸铵对照品(必要时与供试品同
法处理)的图谱一致。
【检查】溶液的澄清度与颜色 取本品约0.1g,加 20%乙醇20ml溶解并稀释至100ml,
溶液应澄清无色;如显色,与橙黄色 0.5 号标准比色液(通则 0901 第一法)比较,不得更深。
有关物质 照高效液相色谱法(通则 0512)测定。取本品适量,精密称定,加流动相溶解并定量稀释制成每 1ml 约含甘草酸铵 1mg 的溶液,作为供试品溶液。精密量取供试品溶液适量,加流动相稀释制成每 1ml 含甘草酸铵 0.05mg 的溶液,作为对照溶液。系统适用性溶液、色谱条件、系统适用性要求见含量测定项下。精密量取供试品溶液与对照溶液各 10ul,分别注入液相色谱仪,记录色谱图至主峰保留时间的 3 倍。供试品溶液色谱图中如有与杂质 I(相对保留时间约 0.7)保留时间一致的色谱峰,杂质 I 不得大于对照溶液除溶剂峰外各色谱峰面积之和的 1.14 倍(5.7%);其他单个杂质不得大于对照溶液除溶剂峰外各色谱峰面积之和的 0.4 倍(2.0%);其他各杂质峰面积的和不得大于对照溶液除溶剂峰外各色谱峰面积之和的 1.6 倍(8.0%)。
乙醇 取本品约 0.1g,精密称定,置顶空瓶中,精密加入 0.1mol/L 氢氧化钠溶液 5ml 使溶解,密封,作为供试品溶液。另取乙醇对照品适量,精密称定,用 0.1mol/L 氢氧化钠溶液溶解并定量稀释制成每 1ml约含乙醇 1mg 的溶液,精密量取 5ml,置顶空瓶中,密封,作为对照品溶液。照气相色谱法(通则 0521)试验,用 6%氰丙基苯基-94%二甲基聚硅氧烷(或极性相近)为固定液的毛细管柱;起始温度为 40℃,维持 1 分钟,以每分钟 15℃的速率升温至 200℃,维持 5 分钟;进样口温度为 220℃;检测器温度为 250℃;顶空瓶平衡温度为 90℃,平衡时间为 30 分钟。
取供试品溶液与对照品溶液分别顶空进样,记录色谱图。按外标法以峰面积计算,即得。水分 取本品,照水分测定法(通则 0832 第一法 1)测定,含水分不得过 6.0%。炽灼残渣 取本品 1.0g,依法检查(通则 0841),遗留残渣不得过 0.5%。
【含量测定】照高效液相色谱法(通则 0512)测定。用十八烷基硅烷键合硅胶为填充剂;以乙腈-冰醋酸-水(38:1:61)为流动相,检测波长为 254nm。取甘草酸铵对照品(含 18α-甘草酸铵和 18β-甘草酸铵)适量,加流动相溶解并稀释制成每 1ml 约含 1mg 甘草酸铵的溶液,作为系统适用性溶液。量取 10ul 注入液相色谱仪,记录色谱图,18α-甘草酸铵和 18β-甘草酸铵(相对保留时间分别约为 1.5 和 1.0)的分离度应不低于 2.0。取本品适量,精密称定,用流动相溶解并定量稀释制成每 1ml 中约含 0.5mg 甘草酸铵的溶液,作为供试品溶液,精密量取 10ul 注入液相色谱仪,记录色谱图。另取 18β-甘草酸对照品适量,用流动相溶解并定量稀释制成每 1ml 中约含 0.5mg 18β甘草酸的溶液,作为对照品溶液,同法测定。按外标法以峰面积分别计算 18α-甘草酸铵和 18β-甘草酸铵的含量,将结果乘以 1.02,并计算总和,即得。
【类别】 甜味剂。
【贮藏】 密封保存。
【标示】 应标明乙醇含量。
注:①本品有引湿性。②为满足制剂稳定性和安全性要求,必要时可对元素杂质铅进行
控制。2025 年 1 月
起草单位:广东省药品检验所 联系电话:020-81853846
复核单位:武汉药品医疗器械检验所
甘草酸铵药用辅料标准草案修订说明
1.名称 根据征集样品的实际情况,并结合国外药典规定拟定。
2.性状 根据征集样品的实际情况,并结合国外药典规定拟定。
3.鉴别 采用理化、液相和红外鉴别方法进行鉴别,根据征集样品实际情况并结合国药药典规定拟定。
4.检查
4.1溶液的澄清度与颜色 参考国外药典并结合中国药典通则《0901溶液颜色检查法》拟定。
4.2 有关物质 由于甘草酸皂苷 G2(24-羟基-甘草酸)存在于甘草原料中,在目前主流的甘草酸铵中提取工艺中难以完全去除。对 24-羟基-甘草酸进行控制具有必要性。参考国外药典拟定。
4.3 乙醇 由于本品的主要工艺为乙醇浸提,且乙醇与甘草酸铵可能形成溶剂化结晶,乙醇的去除需要特定工艺,故有必要对本品乙醇含量进行考察。鉴于本品主要作为甜味剂,在使用过程中添加量较少,乙醇为 3 类溶剂,根据中国药典与 ICHQ3C 协调的相关原则,在标准中不进行限度控制,但由于此项目结果需用于含量计算,故需在标示项下标示。
4.4 水分 由于本品具有引湿性,如果未能妥善保管可能会导致水分吸收,影响样品纯度和质量稳定性,对本品水分控制具有必要性。参考国外药典拟定。
4.5 炽灼残渣 根据征集样品的实际情况,并结合国外药典规定拟定。
5.含量测定:根据征集样品的实际情况,并结合国外药典规定拟定。
6.类别参考国药药典及《药用辅料手册》拟定。
7 贮藏由于本品具有引湿性,根据样品情况及参考国外药典,拟定密封保存。
8.标示由于乙醇测定结果需用于含量计算,故拟定在标示项下进行标示。
来源:药典委
原文下载:![]() 甘草酸铵药用辅料标准草案公示稿.pdf
甘草酸铵药用辅料标准草案公示稿.pdf

 冀公网安备 13010802000997号
冀公网安备 13010802000997号 微信扫一扫
微信扫一扫