
在全球药品监管趋严和儿童用药安全备受关注的背景下,儿童安全盖(Child-Resistant Closure, CRC)已成为口服液体制剂等儿科用药包装的强制性要求。然而,面对中国、美国、欧洲这三大主要医药市场,制药企业常因错综复杂的标准体系而感到困惑。中国YBB、美国USP、欧洲EP三大标准体系在核心理念、测试方法和合规路径上既有共通之处,又存在关键差异。本文将为您系统梳理与深度对比,并提供清晰的全球市场合规策略。
一、中国标准体系:YBB与GB/T 25163-2025的整合与升级
中国的儿童安全盖标准体系以国家药包材标准(YBB)和国家标准GB/T 25163为核心,并整合于《中国药典》的宏大框架之下。
1. 法规框
架与核心标准
《中国药典》2025版:作为药品标准的根本大法,其构建的“1+4+58”药包材标准体系是总纲领。其中,《9624 药品包装用塑料材料和容器指导原则》明确要求防儿童开启功能需通过认证。
GB/T 25163-2025:这是防止儿童开启包装的基础性通用标准。新版标准于2025年6月30日发布,2026年1月1日强制实施,修改采用了国际标准ISO 8317:2015,标志着中国标准与国际全面接轨。其核心要求是:在无演示的5分钟内,至少85%的42-51月龄儿童无法开启;演示后,整个10分钟内至少80%的儿童无法开启;同时,90%的50-70岁成人能在5分钟内开启并重新盖紧。
YBB系列标准:作为具体的产品和方法标准,如YBB系列中对口服液体药用瓶盖的密封性、扭矩等有详细规定。2025版药典实施后,方法类标准以药典为准,但YBB品种标准仍是质量控制的重要依据。
2. 测试与质量控制重点
中国体系特别强调密封完整性和扭矩控制。例如,YBB标准要求进行负压法密封性测试(如-27kPa维持2分钟),并对扭矩测试的精度、环境温湿度控制、数据管理(如要求审计追踪)提出了更细致的要求。对于多次开启后的性能,新规增加了“二次开启扭矩衰减率≤15%”的要求。
二、美国标准体系:USP <671>与强制性法规的联动
美国市场对儿童安全包装的要求以联邦法规的强制性和药典标准的专业性相结合为特点。
1. 法规框架与核心标准
《毒物预防包装法案》(PPPA)及16 CFR §1700.20:这是法律强制层面的要求,由美国消费品安全委员会(CPSC)监管。它规定了防止儿童开启的特殊包装的测试程序和要求,适用范围涵盖药品、化学品、家用清洁剂等多种危险品。
美国药典通则〈USP 〈671〉:这是针对药品包装容器性能的专业标准。它主要关注包装的物理化学性能,如密封性、阻隔性(水蒸气透过量)等。虽然USP〈671〉本身不直接规定儿童安全测试流程,但符合PPPA的儿童安全包装必须同时满足USP对容器性能的要求,二者是并行且互补的关系。
2. 测试与认证特点
美国的测试同样基于儿童(42-51个月)和老年人(50-70岁)两组人群的实证测试,要求与ISO 8317及GB/T 25163基本一致。其独特之处在于法规的强制性和广泛的适用性,并且CPSC拥有直接的执法权。产品进入美国市场,必须通过CPSC认可的实验室进行测试并取得合规证明。
三、欧洲标准体系:EP与EN14375的分工与协调
欧洲体系以欧洲药典(EP)为药品质量基准,以EN标准为产品安全性能的具体规范,两者分工明确。
1. 法规框架与核心标准
欧洲药典(EP):EP主要规定药品的质量、安全性和有效性,对包装材料有通用要求(如生物相容性、保护性),但未专门详细规定儿童安全测试方法。
EN 14375:2016:这是专门针对药品用不可重新封闭包装(如泡罩、条状包装)的儿童安全标准。它被欧盟各国采纳为国家标准(如BS EN 14375, DIN EN 14375)。
EN ISO 8317:2015:这是针对可重新盖紧包装(如压旋盖药瓶)的儿童安全标准,等同采用国际标准ISO 8317。
EN 862:适用于非药品危险品的不可重新封闭包装标准。
2. 测试与市场准入
欧洲标准对测试人群的性别和年龄分布有更严格的规定。例如,EN 14375要求成人测试组中,50-70岁的100名受试者需按年龄段分组,且每组中女性比例必须达到70%。这更科学地模拟了药品的主要使用者(老年女性)群体。产品进入欧盟市场,通常需要获得由公告机构(Notified Body)颁发的EN标准符合性证书。
四、核心异同对比一览表
| 对比维度 | 中国 (YBB / GB/T 25163) | 美国 (USP & PPPA) | 欧洲 (EP & EN标准) |
| 核心法规/标准 | 《中国药典》2025版、GB/T 25163-2025、YBB标准 | 《美国药典》〈USP 〈671〉、16 CFR §1700.20 (PPPA) | 欧洲药典 (EP)、EN 14375 (不可重封)、EN ISO 8317 (可重封) |
| 法律性质 | 国家标准(GB/T)为强制,药典为药品法定标准 | PPPA为联邦法律,强制;USP为行业权威标准 | EN标准在欧盟成员国通常具有法规引用地位,事实强制 |
| 测试人群要求 | 儿童:42-51个月;成人:50-70岁 | 同左 | 儿童:42-51个月;成人:50-70岁,且要求特定年龄分组和70%女性比例 |
| 性能合格标准 | 儿童:无演示≤15%开启(5分钟);总测试≤20%开启(10分钟)。成人:≥90%开启(5分钟)并复现 | 与ISO 8317一致,同左 | 与ISO 8317一致(EN ISO 8317)。EN 14375针对不可重封包装有类似要求 |
| 关注重点 | 强调与药典整合,注重密封性、扭矩等理化性能的量化控制 | 法规符合性与容器性能并重,强调CPSC的执法权威 | 标准符合性认证,测试程序严谨,特别关注老年女性的可用性 |
| 适用产品范围 | 药品(特别是口服液体制剂)及其他危险品 | 药品、化学品、家用产品等广泛危险品 | EN 14375专用于药品;EN 862用于非药品;EN ISO 8317用于可重封包装 |
五、全球市场合规策略建议
面对多重要求,制药企业可采取以下策略实现高效合规:
1.“就高不就低”的融合设计
在产品设计初期,即以最严格的标准维度作为设计输入。例如,同时满足中国对扭矩精度的要求、美国对法规的强制性以及欧洲对测试人群细分的标准。采用经过ISO 8317认证的成熟盖型设计,是通往全球市场的基础通行证。
2.一体化测试与报告
规划全球申报时,可委托具有国际互认资质(如ILAC)的实验室进行测试。一份设计良好的测试方案和报告,可以同时或稍作调整后用于支持中国、美国、欧盟的注册申报,避免重复测试,节省时间和成本。
3.构建模块化注册资料
在准备注册文件时,将儿童安全盖的验证资料构建成独立、完整的模块。包括:
设计依据:说明符合GB/T 25163、ISO 8317等标准。
测试报告:提供由权威实验室出具的儿童防护性能测试报告。
相容性研究:依据USP〈1663〉/〈1664〉或EP 3.1/3.2及中国药典要求,完成可提取物与浸出物研究。
功能测试:提供密封性、扭矩、多次开启耐久性等数据。
4.供应链与质量管理
选择包材供应商时,确保其质量管理体系能持续稳定地生产符合多国标准的产品。在质量协议中明确原材料、工艺变更的管控要求,并定期进行供应商审计。
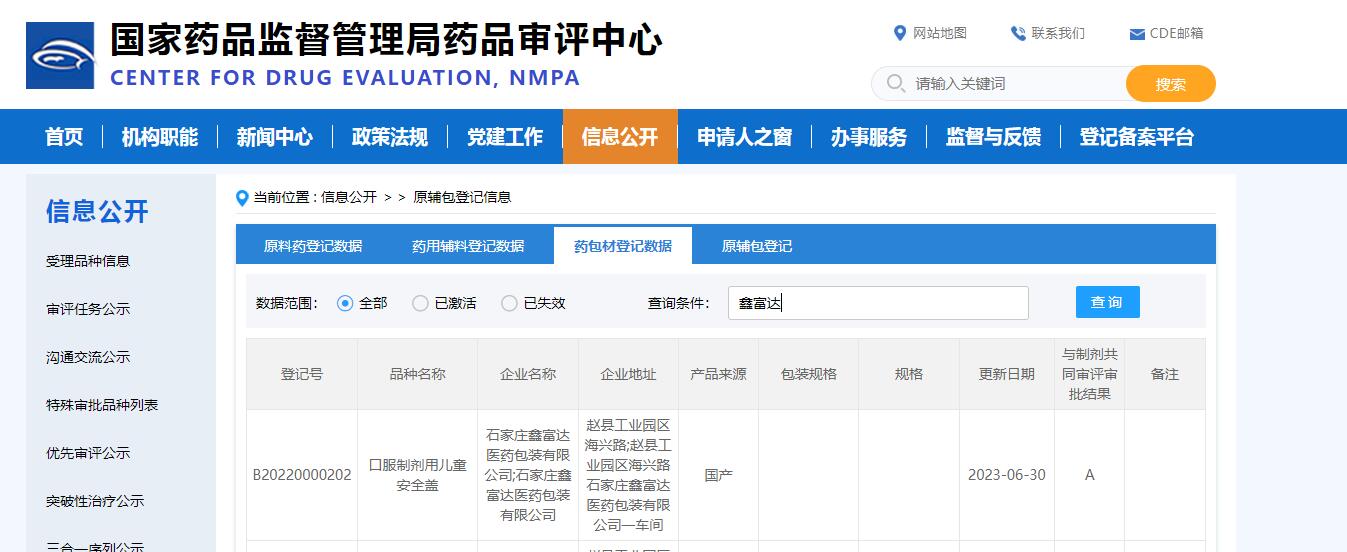
口服液体药用聚丙烯压旋盖CDE登记号为A状态
中国YBB、美国USP、欧洲EP三大标准体系共同构筑了儿童用药安全的全球防线。其核心目标一致——在“儿童难开”与“成人易用”间取得完美平衡,但具体路径和侧重点各有特色。对中国制药企业而言,深入理解这些异同,绝非增加负担,而是开拓全球市场的必修课。
在法规日益趋同的今天,采用国际主流标准(如ISO 8317) 进行研发和验证,并在此基础上满足特定市场的细微要求,是实现“一次开发,全球申报”的最优解。将儿童安全盖的合规工作,从被动的成本项转变为主动的产品价值与竞争力,方能在保障儿童用药安全的伟大使命中,赢得市场的尊重与先机。

 冀公网安备 13010802000997号
冀公网安备 13010802000997号 微信扫一扫
微信扫一扫