
随着国家对儿童用药安全重视程度的不断提升,药品包装的儿童安全防护已成为法规监管的核心焦点。对于口服液体制剂,特别是氨溴特罗、氨溴索等儿科常用药,儿童安全盖(Child Resistant Cap,简称CRC盖)的应用已从“推荐”逐步走向“强制”。本文将深度解读CDE及相关机构的最新法规要求,明确企业合规的实施路径与时间表,为制药企业的研发与质量人员提供清晰的行动指南。
一、法规体系升级:从推荐标准到强制要求的转变
长期以来,我国儿童安全包装主要依据2010年发布的推荐性国家标准《防止儿童开启包装——可重新盖紧包装的要求与试验方法》(GB/T 25163-2010)。该标准虽为行业提供了技术依据,但并未强制要求所有儿童用药必须采用。许多企业仅通过药盒警示语等方式履行最低限度的安全提示义务。
这一局面正在发生根本性改变。2025年,国家标准化管理委员会发布了新版GB/T 25163-2025《防止儿童开启包装 可重新盖紧包装的要求与试验方法》,该标准已于2025年6月30日正式发布,并将于2026年1月1日起强制实施。新标准与国际标准ISO 8317:2015进一步接轨,提升了我国儿童安全包装要求的国际通用性与实践可行性。
与此同时,2025年版《中华人民共和国药典》已于2025年3月25日正式颁布,并定于2025年10月1日起实施。药典作为国家药品标准的法定核心,其相关要求具有强制执行力。对于口服液体制剂,药典在包装材料、密封性能、标识等方面提出了更系统、更严格的规定。
二、核心强制要求解析:“儿童难开,成人易用”的双重标准
儿童安全盖的设计必须同时满足防护性与可用性的平衡,其核心强制要求可概括为“儿童难开,成人易用”的双重标准。
1. 儿童防护性能要求
在规定的测试条件下,85%以上的5岁以下儿童在5分钟内无法自行开启包装。这要求CRC盖必须采用有效的防开启机制,如目前主流的压旋式设计,通过需要同时完成“下压”与“旋转”的复合动作,利用幼儿手部协调能力尚未发育完全的特点来提供防护。
2. 成人易用性要求
在确保儿童安全的同时,包装必须便于目标使用者(主要是成年监护人)正常开启。标准要求70%以上的老年人能够正常开启并使用。这要求企业在设计时需充分考虑人机工程学,优化盖子的直径、纹理、按压力度等参数,避免因过度追求安全性而导致老年人或手部功能受限者开启困难。
3. 材料与相容性要求
直接接触药品的CRC盖材料(通常为聚丙烯PP或聚乙烯PE)必须符合药典对药用包装材料的通用要求,并需开展完整的包材相容性研究,包括可提取物与浸出物评估,确保其不会引入安全性风险或影响药品稳定性。
口服液体药用高密度聚乙烯瓶60ml压旋盖
三、明确实施时间表:企业合规的最后期限
面对法规升级,药品上市许可持有人(MAH)必须清晰把握以下关键时间节点,制定切实可行的合规计划。
关键时间节点
2025年10月1日:2025版《中国药典》正式实施起始日。自此日起,所有新提交的药品注册申请(包括新药、仿制药、补充申请等),其申报资料中关于包装系统的研究数据必须完全符合新药典的相关要求。
2026年1月1日:新版国家标准GB/T25163-2025正式强制实施日。所有生产上市的、适用范围内的儿童药品包装,其儿童安全性能必须符合该标准的最新测试方法与接受标准。
2026年4月1日:对于在2025年10月1日前已按原标准批准上市的药品,法规给予了6个月的过渡期。这意味着最晚在2026年4月1日前,所有已上市口服液体制剂(特别是儿童用药)的包装必须完成升级或变更,以确保符合2025版药典的全部要求。
针对不同产品的合规路径
在研及新报产品:必须直接按照最新标准进行包材选择、相容性研究及注册申报。
已上市产品:需立即启动包装系统变更研究,按照《药品上市后变更管理办法》的要求,评估变更等级(通常涉及中等变更),开展对比研究与稳定性考察,并按时提交备案或补充申请。

口服液体药用聚丙烯瓶100ml
四、合规应对策略:从研发到生产的全链条行动建议
1. 研发阶段:基于QbD理念的包材选型与验证
企业应从产品研发初期就引入质量源于设计(QbD)理念,将儿童安全作为包装系统的关键质量属性(CQA)。针对氨溴特罗、氨溴索等具体品种的处方特性(pH、粘度、辅料),科学选择CR盖的材质与结构,并完成完整的功能测试(密封性、开启力、重复开启性)与相容性研究。
2. 注册申报:完善关联审评资料
在药品注册申报时,应按照关联审评审批要求,准备详尽的包材研究资料。重点证明所选CR盖符合GB/T 25163-2025的儿童防护与成人易用标准,并提供其与药品相容、不影响产品稳定性的充分证据。
3. 生产质量:工艺验证与持续控制
将普通旋盖生产线改造为适配CR盖的生产线,需重点关注旋盖扭矩控制的工艺验证。建立合理的扭矩标准范围,确保既能达到有效密封,又不会导致开启力超标。同时,应建立在线检测机制,如采用真空衰减法等对容器密封完整性(CCI)进行100%监控。
4. 供应链管理:强化供应商审计
将CRC盖的儿童安全性能纳入供应商质量协议,对供应商的生产工艺、质量控制体系及变更管理进行严格审计,确保包材性能的持续稳定。
五、行业展望:超越合规,迈向智能与绿色未来
法规的强制要求是底线,而非上限。领先企业正着眼于未来趋势,将儿童安全盖与物联网技术结合,开发智能瓶盖,实现服药提醒、剂量记录等功能,提升用药依从性。同时,采用可回收材料(如消费后回收聚丙烯)制造环保CRC盖,平衡产品保护与环境责任,已成为行业的重要发展方向。
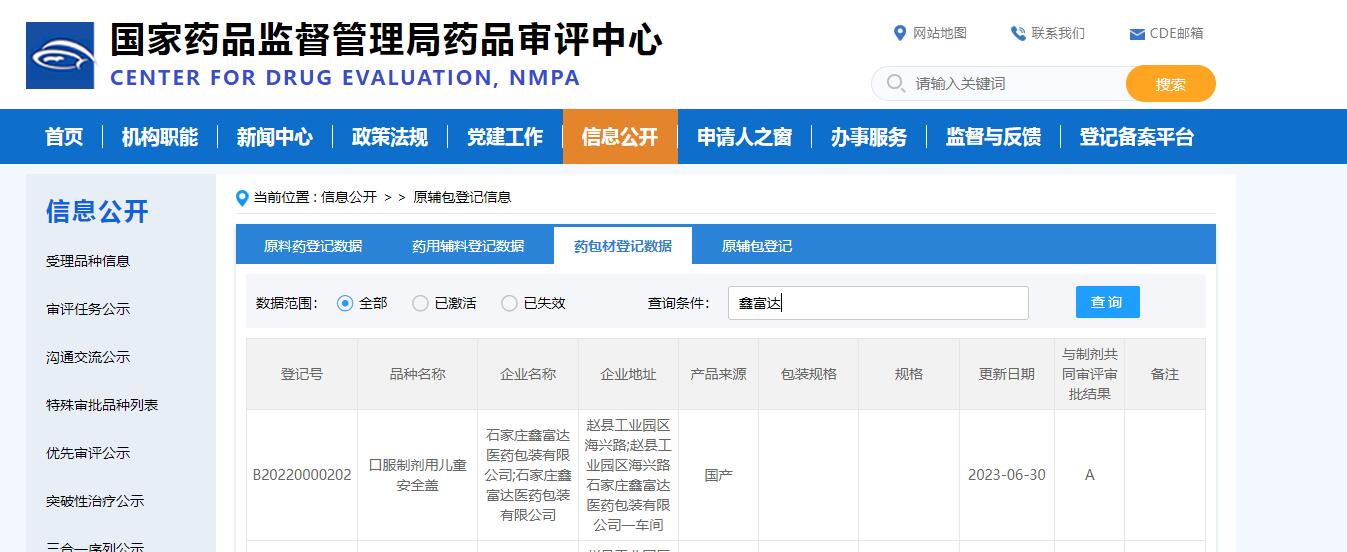
口服液体药用聚丙烯压旋盖CDE登记号为A状态
儿童用药安全无小事,CDE及相关国家机构通过法规标准升级,正强力推动儿童安全盖在口服液体制剂中的普及应用。明确强制要求与实施时间表,是企业履行社会责任、保障儿童健康、规避合规风险的必然选择。制药企业应即刻行动,系统规划,将儿童安全包装的合规工作嵌入从研发到上市后管理的全生命周期,以此为契机,提升产品核心竞争力,赢得市场与社会的双重认可。

 冀公网安备 13010802000997号
冀公网安备 13010802000997号 微信扫一扫
微信扫一扫